
Trozo de metal oxidado (corroído)
Para que exista una reacción redox, en el sistema debe haber un elemento que ceda electrones y otro que los acepte:
- El agente reductor es aquel elemento químico que suministra electrones de su estructura química al medio, aumentando su estado de oxidación, es decir, siendo oxidado.
- El agente oxidante es el elemento químico que tiende a captar esos electrones, quedando con un estado de oxidación inferior al que tenía, es decir, siendo reducido.[1]
Contenido[ocultar] |
[editar] Principio de electroneutralidad
Dentro de una reacción global redox, se da una serie de reacciones particulares a las cuales se les llama semirreacciones o reacciones parciales.- 2 Na+ + 2 Cl− → 2 Na + Cl2
- 2 NaCl → 2 Na + Cl2
Una titulación redox es una en la que un indicador químico indica el cambio en el porcentaje de la reacción redox mediante el viraje de color entre el oxidante y el reductor.
[editar] Oxidación

Oxidación del hierro.
Por ejemplo, en la reacción de formación del cloruro de hidrógeno a partir de los gases dihidrógeno y dicloruro, se da un proceso redox y sin embargo se forma un compuesto covalente.
Estas dos reacciones siempre se dan juntas, es decir, cuando una sustancia se oxida, siempre es por la acción de otra que se reduce. Una cede electrones y la otra los acepta. Por esta razón, se prefiere el término general de reacciones redox.
La propia vida es un fenómeno redox. El oxígeno es el mejor oxidante que existe debido a que la molécula es poco reactiva (por su doble enlace) y sin embargo es muy electronegativo, casi como el flúor.
La sustancia más oxidante que existe es el catión KrF+ porque fácilmente forma Kr y F+.
Entre otras, existen el permanganato de potasio (KMnO4), el dicromato de potasio (K2Cr2O7), el agua oxigenada (H2O2), el ácido nítrico (HNO3), los hipohalitos y los halatos (por ejemplo el hipoclorito de sodio (NaClO) muy oxidante en medio alcalino y el bromato de potasio (KBrO3)). El ozono (O3) es un oxidante muy enérgico:
- Br− + O3 → BrO3−
- 2 NaI + Cl2 → I2 + 2 NaCl
- 2I− → I2 + 2 e−
- Cl2 + 2 e− → 2 Cl
- Ejemplo
- Óxido ferroso: FeO.
- Óxido férrico: Fe2O3
[editar] Reducción
En química, reducción es el proceso electroquímico por el cual un átomo o ion gana electrones. Implica la disminución de su estado de oxidación. Este proceso es contrario al de oxidación.Cuando un ion o un átomo se reduce presenta estas características:
- Gana electrones.
- Actúa como agente oxidante.
- Es reducido por un agente reductor.
- Disminuye su estado o número de oxidación.
- Ejemplo
- Fe3+ + e− → Fe2+
- CH≡CH + H2 → CH2=CH2 (el etino se reduce para dar eteno).
- CH3–CHO + H2 → CH3–CH2OH (el etanal se reduce a etanol).
[editar] Número de oxidación
La cuantificación de un elemento químico puede efectuarse mediante su número de oxidación. Durante el proceso, el número de oxidación del elemento aumenta. En cambio, durante la reducción, el número de oxidación de la especie que se reduce disminuye. El número de oxidación es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un enlace determinado.El número de oxidación:
- Aumenta si el átomo pierde electrones (el elemento químico que se oxida), o los comparte con un átomo que tenga tendencia a captarlos.
- Disminuye cuando el átomo gana electrones (el elemento químico que se reduce), o los comparte con un átomo que tenga tendencia a cederlos.
[editar] Reglas para asignar el número de oxidación
- El número de oxidación de todos los elementos sin combinar es cero. Independientemente de la forma en que se representen.
- El número de oxidación de las especies iónicas monoatómicas coincide con la carga del ion.
- El número de oxidación del hidrógeno combinado es +1, excepto en los hidruros metálicos, donde su número de oxidación es –1 (ej: AlH3, LiH)
- El número de oxidación del oxígeno combinado es –2, excepto en los peróxidos, donde su número de oxidación es –1 (ej.:Na2O2, H2O2).
- El número de oxidación en los elementos metálicos, cuando están combinados es siempre positivo y numéricamente igual a la carga del ion.
- El número de oxidación de los halógenos en los hidrácidos y sus respectivas sales es –1, en cambio el número de oxidación del azufre en su hidrácido y respectivas sales es –2.
- El número de oxidación de una molécula es cero. O lo que es lo mismo, la suma de los números de oxidación de los átomos de una molécula neutra es cero.
[editar] Ajuste de ecuaciones
Todo proceso redox requiere del ajuste estequiométrico de los componentes de las semireacciones para la oxidación y reducción.Para reacciones en medio acuoso, generalmente se añaden:
- en medio ácido iones hidrógeno (H+), moléculas de agua (H2O), y electrones
- en medio básico hidroxilos (OH−), moléculas de agua (H2O), y electrones para compensar los cambios en los números de oxidación.
[editar] Medio ácido
En medio ácido se agregan hidronios (cationes) (H+) y agua (H2O) a las semirreacciones para balancear la ecuación final.Del lado de la ecuación que haga falta oxígeno se agregarán moléculas de agua, y del lado de la ecuación que hagan falta hidrógenos se agregarán hidronios.
Por ejemplo, cuando el Manganeso (II) reacciona con el Bismutato de Sodio.
Ecuación sin balancear:
- Oxidación :

- Reducción :

- Oxidación:

- Reducción:

- Oxidación:
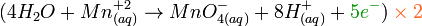
- Reducción:

- Oxidación:

- Reducción:



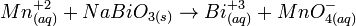


No hay comentarios:
Publicar un comentario